1.
Сумма моментов сил, действующих на блок равна произведению
момента инерции на угловое ускорение
ΣM=I·w
Если
разность натяжения нитей обозначить через ΔF, то момент, создаваемый ими
ΔF·R
ΔF·0.2-98.1=50·2.36
ΔF=1080 Н
2.
Одна
молекула Азота имеет среднюю кинетическую энергию
E=m·v²/2
где m=масса
одной молекулы
m=µ/NA
Поскольку
мы знаем всю кинетическую энергию W
то можно определить количество молекул Азота N
N=W/E
и
полную массу Азота
M=N·m
M=N·µ/NA
M=2·W/v²
M=2·5000/2000²
M=0.0025 кг
M=2.5 г
Из
основного уравнения термодинамики
P=(2/3)·n·Ek
Где n-концентрация молекул
n=N/V
Ek=m·v²/2 – энергия одной молекулы
Учитывая,
что M=N·m
Получим
PV=M·v²/3
V= M·v²/(3·P)
V=0.0025·2000²/(3·250000)
V=0.013 м³
3.
Как
известно, для многоатомных газов
теплоемкость
при изохорном (постоянный объем) процессе равна
Сv=3·R
При
изобарном (постоянное давление) процессе
Cp=4·R
Поэтому
можем рассчитать количество теплоты, полученные при изохорном нагревании
Qv=Cv·ΔT
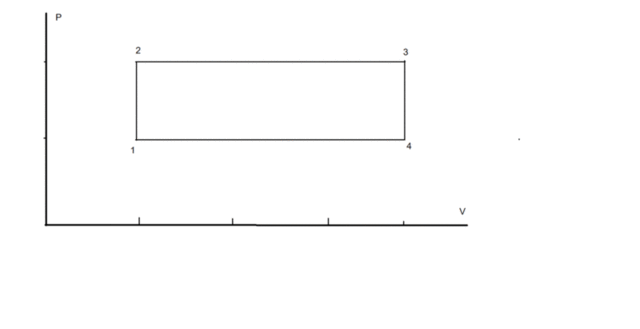
Газ
получает тепло на участке 1-2 и 2-3
Используя
соотношение для изохорного процесса 1-2
P1/T1=P2/T2
P2=2·P1
T2=2·T1
Qv=Cv·ΔT
Qv=Cv·(T2-T1)
Qv=Cv·(2·T1-T1)
Qv=Cv·T1
Qv12=3·R·T1
Аналогично,
для изобарного процесса 2-3
Qp=Cp·ΔT
V1/T2=V2/T3
V2=4·V1
T3=4·T2
Qp=Cp·(T3-T2)
Qp=4·R·(4·T2-T2)
Qp=4·R ·3·T2
Qp=12·R·T2
T2=2·T1
Qp23=24·R·T1
Находим
работу газа
A=ΔP·ΔV
A=(P2-P1)·(V2-V1)
P2=2·P1
V2=4·V1
A=3·P1·V1
P1·V1=R·T1
A=3·R·T1
KKD=A/(Q12+Q23)
KKD=3/(3+24)
KKD =0.11
KKD=11%