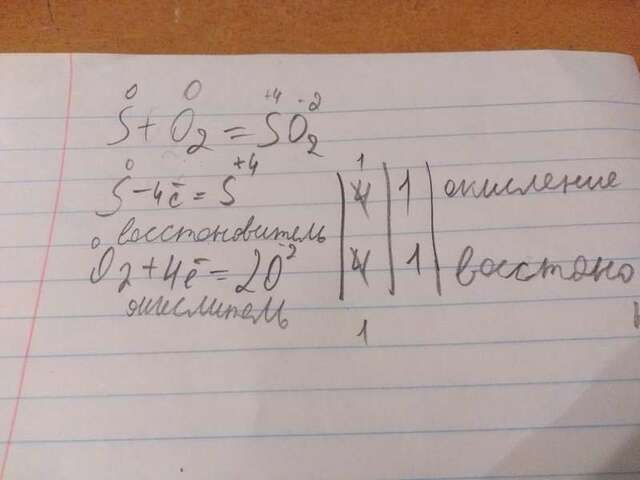№1.
Оксиды:
Na2O, Cl2O7, ZnO, CaO, CO2.
Солеобразующие оксиды:
Na2O (основный оксид);
ZnO (амфотерный оксид);
CO2 (кислотный оксид);
Cl2O7 (кислотный оксид);
CaO (основной оксид).
№2
2K + 2H2O = K2O + 2H2 (↑)
N2O5 + H2O = 2HNO3
BaO + H2O = Ba(OH)2
№3
S -> SO -> H2SO3
1) S + O2 = SO2
2) SO2 + H2O = H2SO3
№4
1) р-я соединения.
2) р-я соединения.
Окислительно - восстановительная реакция (на фотографии).
№5
Свойства атома
водорода, сложных веществ, в состав которых он входит, и самого простого
вещества Н2 в первую очередь определяются электронной конфигурацией
гидрогена. Частица имеет один электрон с Z= (-1), который вращается по
своей орбите вокруг ядра, содержащего один протон с единичной массой и
положительным зарядом (+1). Его электронная конфигурация записывается
как 1s1, что означает наличие одной отрицательной частицы на самой
первой и единственной для гидрогена s-орбитали.
Если описывать
физические свойства водорода кратко, то это бесцветный, малорастворимый
газ с относительной атомной массой равной 2, в 14,5 раза легче, чем
воздух, с температурой сжижения, составляющей -252,8 градуса Цельсия.
№6
Дано:
m р.в.(растворенного в-ва) = 25 гр
w (омега) = 10% = 0,1
Найти:
m р. (растворителя) = ?
Решение.
w = m р.в. / m р-ра (раствора)
m р-ра = m р.в. / w --> m р-ра = 25/0,1 = 250 г
m р. = m р-ра - m р.в --> m р. = 250 г - 25 г = 225 г
Ответ: m р. = 225г
Найдем массу чистой кислоты:
m = 600*0,12 = 72г
Массовая доля находится по формуле:
ω=m(вещ-ва) / m(раствора)
W =  = 0,09 (или 9%)
= 0,09 (или 9%)
(200 мл=200 г)
Ответ: 0,09 (9%)